第一節
新加坡HSA –泰國FDA 監管信賴試點項目
2022.06.01 公共衛生部泰國食品藥品管理局(Thai FDA)醫療器械控制司發布公告,自 2022年6 月 1 日起對風險分類爲 2-4 或 B-D的體外診斷醫療設備(IVD) 或非體外診斷醫療器械 (Non-IVD) 實施泰國 FDA – HSA 新加坡監管信賴計劃。
泰國 FDA – HSA 新加坡監管信賴是監管機構之間的一項加速醫療器械注冊計劃,向制造商或進口商提出縮短注冊期限的提議。由于泰國 FDA 醫療器械控制部已被新加坡衛生科學局機構認可爲參考機構,在該計劃中,泰國 FDA 將與衛生科學局機構合作評估醫療器械的性能和安全性,新加坡的評估報告。即已獲得 HSA醫療器械許可證並希望參與監管信賴計劃的新加坡注冊人可以允許 HSA向泰國 FDA 提交醫療器械評估報告。
參與條件
1. 在新加坡注冊的醫療器械,以及
2. 作爲體外診斷醫療設備 (IVD) 或非體外診斷醫療器械 (Non-IVD) 的風險分類 2-4 或 B-D。
優點
1.降低泰國FDA注冊費,專家評審過程,最高可免除 53,000 泰铢的費用(取決于其風險分類);
2、技術文件審核時間周轉時間將從 150 個工作日減少到 60 個工作日。
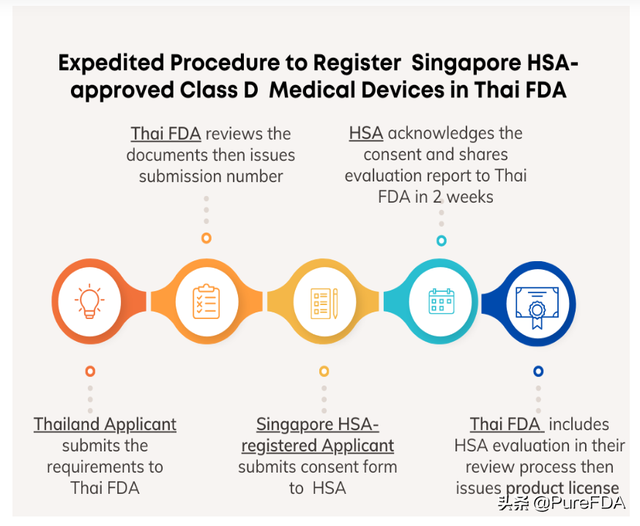
操作步驟
1.提交參與監管信賴計劃的申請信;
2. 制造商或進口商通過電子版提交醫療器械許可申請,需要提交文件如下:
1) 以通用提交技術文件模板 (CSDT) 形式的注冊文件,即與用于在 HSA 機構注冊的CSDT 文件相同,
2) 經HSA機構授權的變更通知文件(如有),
3) 要求參與監管信賴計劃的申請信,
4)新加坡HSA批准醫療器械注冊證明。
3. 在電子提交系統中收到申請號後,新加坡的注冊人(擁有 HSA 的醫療器械許可證的公司)簽署泰國 FDA 和新加坡 HSA Reliance 同意書範本 (Consent Form) 允許 HSA 向泰國食品和藥物管理局醫療器械控制司提供醫療器械提供評估報告。
4. 泰國 FDA 官員將請求發回給制造商或進口商並附上電子提交系統中的同意書。
其實新加坡 HSA-泰國 FDA 監管信賴試點項目早在幾年前就啓動了。爲探索解決監管機構面臨的新技術發展等挑戰,並加強患者獲得醫療器械的機會,新加坡 HSA 和泰國 FDA 在亞太醫療技術論壇 (APACMed) 的支持下,在雙方建立信任後于 2020 年 9 月啓動了監管信賴試點項目。
在 COVID-19 大流行之前,泰國 FDA 能夠派遣三名評估人員在新加坡與 HSA 共度兩周,以熟悉 HSA 的評估方法。作爲該項目的一部分,該試點項目也是 HSA 和泰國 FDA 爲能力建設目的就目標類別的醫療器械交換信息的機會。在試點項目開始之前,HSA 與泰國 FDA 簽署了保密協議,以允許兩個當局自由地相互分享提交相關信息。
2020 年 9 月該項目實施第一階段試點,泰國 FDA 提議以先到先得的方式接受 12 份申請。該試點對整個行業開放。
2021年8月,泰國 FDA 發布公告,泰國 FDA 已被新加坡衛生科學局機構認可爲參考機構,在此計劃中,泰國 FDA 將與新加坡衛生科學局機構合作評估醫療器械的性能和安全性,出具評估報告。這是首次全面開放,參與條件爲:
1. 已在新加坡注冊的醫療器械,以及
2.風險分類爲4或D的體外診斷醫療設備 (IVD) 或非體外診斷醫療器械 (Non-IVD)。
2022年6月,泰國 FDA 再次發布公告,將監管信賴計劃的適用産品範圍拓展到風險分類爲 2-4 或 B-D 的體外診斷醫療設備 (IVD) 或非體外診斷醫療器械 (Non-IVD)。
第二節
監管信賴的起源
監管信賴的概念最先由世界衛組織WHO提出,其在2020年6月出版的《醫療産品監管中的良好信賴實踐:高級原則和考慮》中定義了監管信賴的各種概念。監管信賴是指權威機構(“信賴機構”)完全或部分信賴另一個市場(“參考機構”)或受信任的機構(如世界衛生組織 (WHO))做出的評估和/或決定對于醫療産品的審批。
監管信賴的最基本形式是利用另一個監管機構已經完成的工作來支持決策過程並保持醫療産品批准的獨立性。更高級的信賴形式是正式接受另一個監管機構根據條約或相互承認等協議做出的決定,而無需重複任何評估。
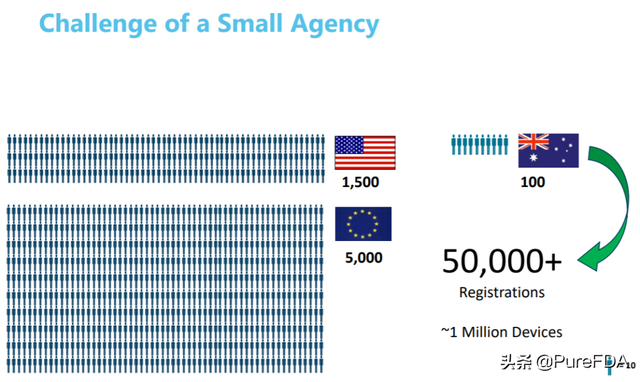
監管信賴的必要性
1. 監管機構壓力,尤其是小的監管機構
2. 新技術的發展
3. 公共衛生安全的威脅
我們已知的監管信賴計劃有醫療器械單一審核計劃 (MDSAP, Medical Device Single Audit Program),該計劃允許對滿足多個監管管轄區要求的醫療器械制造商的質量管理體系進行單一監管審核。審核由參與的監管機構授權和認可的審核組織進行,以根據 MDSAP 要求進行審核。泰國-新加坡的監管信賴項目也是一個典型示範。
考慮到每個國家或者區域法律,法規的相似性以及差異的識別,評估如何去鼓勵國家或者區域間的信任,以及策略的優先級,完全的監管信賴是很難的。但是,如果我們想提高效率和獲得健康産品的機會,我們都必須優先考慮監管信賴,即使是部分信賴。