來源:英倫大叔
近日,一篇名爲《疫苗之王》把疫苗安全的問題推到風口浪尖。長生生物的狂犬疫苗問題、問題疫苗流向、問題疫苗批次,輿論嘩然。
造假疫苗公司——長生生物股份有限公司的老總高俊芳的兒媳隋嘉琪生活有多奢侈。兒子張洺豪的養的小三,簡直是外圍女上位的典範,未婚先孕生了個女兒,擠下原配當了正妻。愛馬仕買起來,香奈兒買起來,用中國兒童的健康換來的奢侈真的可以安心享受?#長生生物被罰344萬#這罰款的334萬,抵得過她買幾個包的錢?
引網友衆怒紛紛前去這位兒媳@隋嘉琪_Athena 微博留言,結果隋嘉琦關閉評論。現在已經刪除所有微博…
該藥企2017年年報,長春長生的營業收入爲15.39億元,淨利潤5.87億元…
這些錢如果是數字的話,我們還很難想像,但是如果換成圖片,大概清楚了。
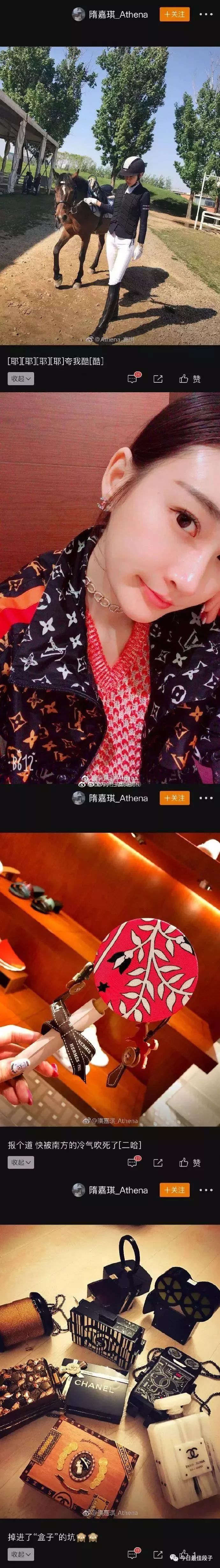
網友截圖小三微博曬圖如下,均是奢侈品,令人眼花缭亂,或者觸目驚心!
擺拍馬場,買奢侈品全套,這不是貧窮限制了所有人的想象力,是良心被豬油蒙蔽!
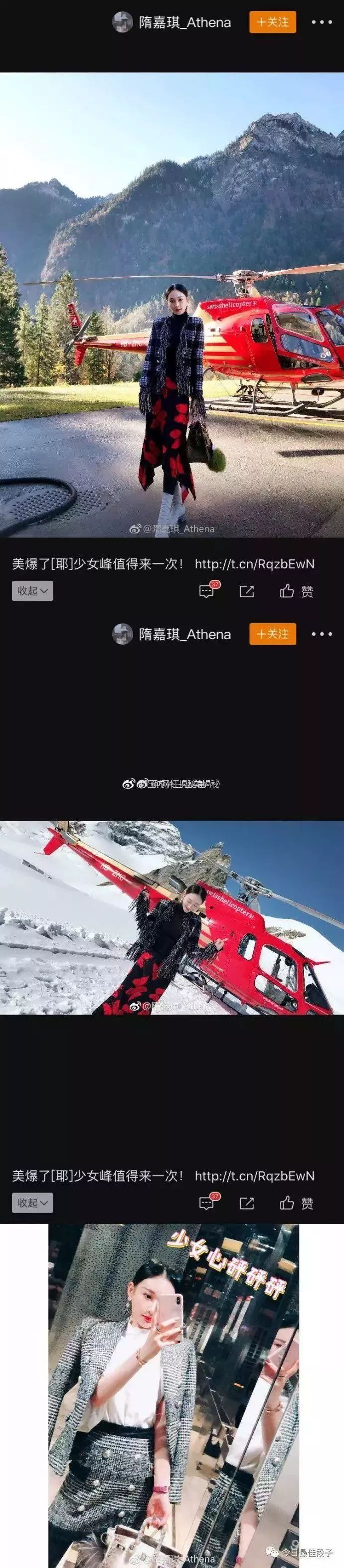
登山靠步行?不用,有直升機接送。
當孩子咬著牙,閉著眼睛害怕打針接種疫苗時,她在買買買,有什麽忌諱:只要貴的。
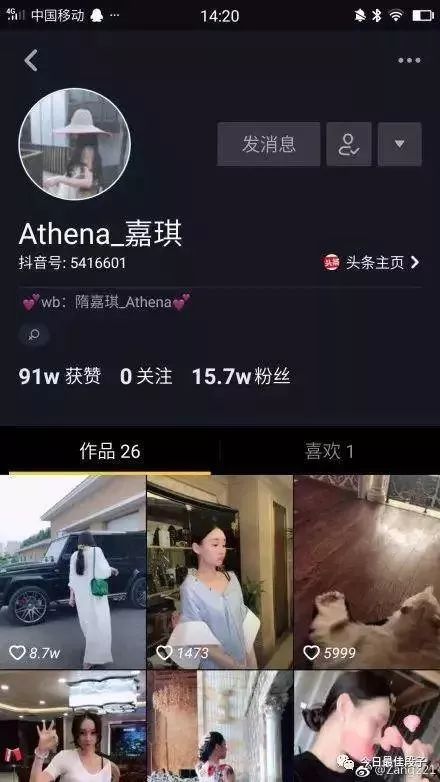
這是隋嘉琪抖音的主頁,全是炫的豪車
根據douyin號去搜索,不要懷疑,就是她
已經刪除全部內容
只留下一個升國旗的視頻,都知道現在這招管用,小三是何等諷刺和囂張!
造假疫苗一事持續發酵。而事件背後的長春長生是長春生物的子公司,系國內狂犬病疫苗第二大企業。據統計,長生生物曾經過19次股權轉讓和2次增資,從國企最終成爲民營企業。此外,這並非它首次出現疫苗生産問題!!
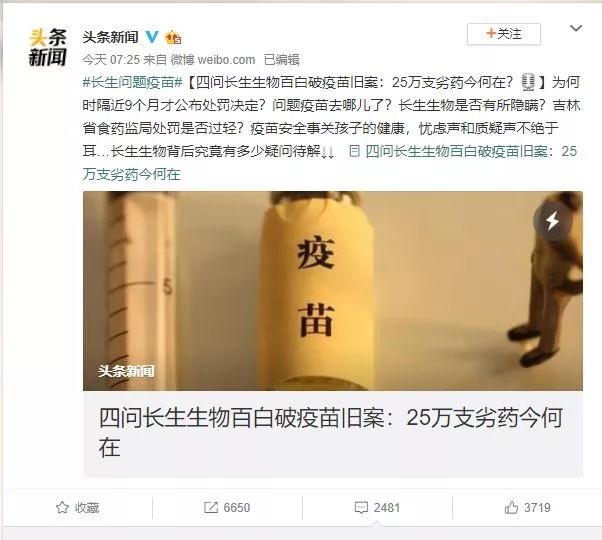
至今仍有25萬支劣藥下落不明,這可是與25萬兒童性命相關的大事
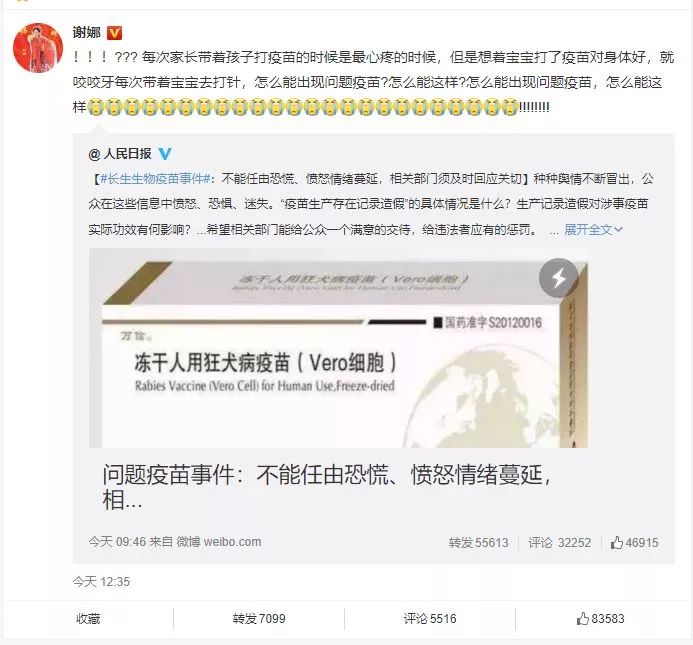
謝娜發微博
從此出國又多了一項任務!
強生爽身粉被罰47億美元!
對于涉事百白破疫苗,吉林省食藥監局處罰決定書顯示,共沒收違法所得85.88萬元,並處違法生産藥品貨值金額三倍罰款258.4萬元。
25萬支問題疫苗,加起來才罰了344.29萬元,處罰是否過輕?
面對這種新聞,網友最多的回複,都是問句!
相關部門是哪個部門?底線到底在哪裏?!已經打的請問該怎麽辦?不應該槍斃這些殺人惡魔嗎?
除了問,我們能怎麽辦?
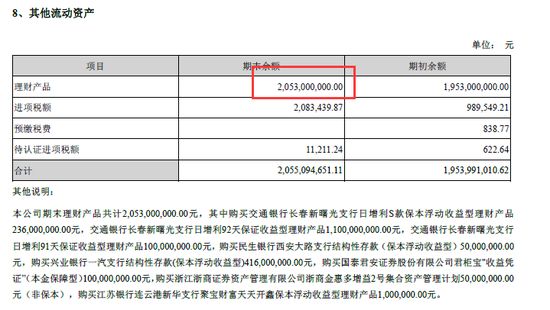
20億資金理財,研發投入僅1.2億。
先是被查出狂犬病疫苗生産記錄造假,隨後又因“吸附無細胞百白破聯合疫苗”(簡稱“百白破”)檢驗不符合規定被罰沒344萬元……長生生物的疫苗“造假”事件,再次刺痛了大家敏感的神經。
家長們紛紛翻看自家孩子的疫苗本,不少人發現,自己孩子接種的疫苗,正是出自長春長生(即長生生物的子公司),而且不止一個種類。
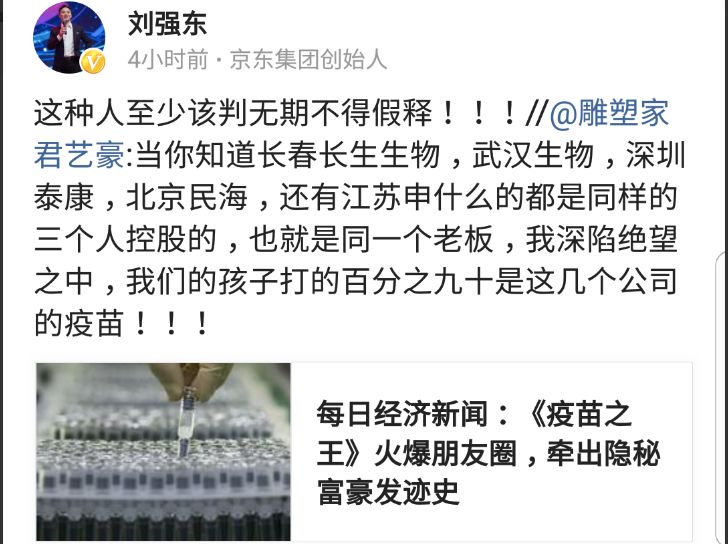
同樣是作爲一位父親,京東創始人劉強東也沒能忍住,他在每日經濟新聞的一篇報道上評價道:
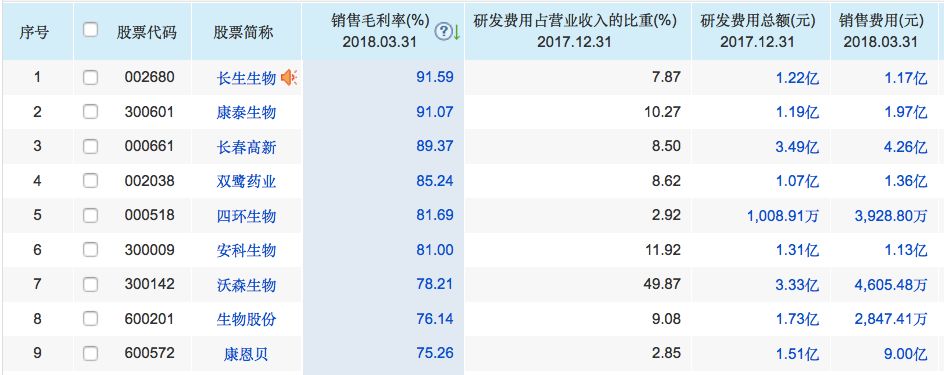
查看長生生物的財務報告不難發現,疫苗的確是個非常賺錢的生意,在疫苗相關上市企業中,長生生物以91.59%的毛利率占據行業首位,比貴州茅台的毛利率(91.31%)還高。
20億資金理財,研發投入僅1.2億
查詢同花順數據發現,A股52家以疫苗爲主營産品的上市公司,今年一季度銷售毛利率平均數高于50%,這一水平已經超過A股大部分行業。
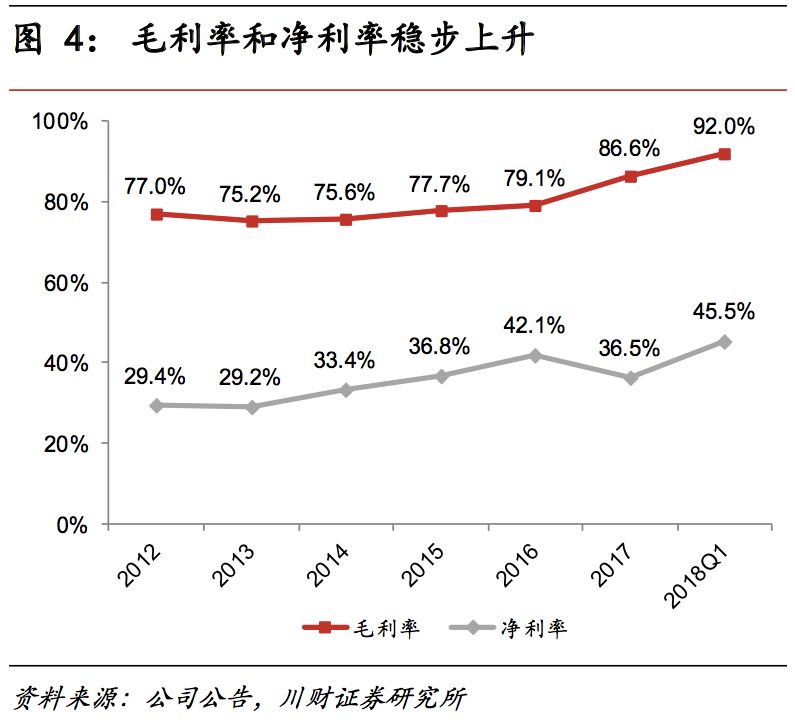
民生證券研報分析稱,“高壁壘、高投入、高周期、高毛利”是疫苗行業的普遍特征。
高壁壘
疫苗行業屬于高度行政監管行業,從研發、生産、流通、銷售和售後安全等各個環節都受政府主管部門嚴格監管和控制。相對于傳統中藥和化藥行業,疫苗(生物制品)行業整體技術水平相對較先進,法律法規相對更嚴格,生産條件也更爲嚴苛。
高周期
疫苗行業與其他制藥企業同樣受制于漫長的研發周期。國內新藥研發周期在8-10年,從研發基本結束到上市一般需要5年以上的時間。
高投入,高毛利
雖然疫苗行業的固定支出大,廠房車間、培養與純化設備折舊成本與銷售成本不容忽視。但是,生産所需外部能源僅包括水電和蒸汽,而細胞培養價格低廉,主要原材料成本在包材和個別特殊原材料(如小牛血清)。
雖然整個疫苗行業都是高毛利率,但長生生物的表現尤爲突出——其以91.59%的毛利率占據行業首位,比貴州茅台91.31%的銷售毛利率還高。
相比毛利率,長生生物的研發投入要遜色得多。2017年,長生生物2017年的研發費用僅1.22億元,占收入的比例爲7.87%;而長春高新爲8.5%,康泰生物爲10.27%,沃森生物更是高達49.87%!
和國外疫苗巨頭相比,長生生物的研發投入也顯得頗爲“克制”。葛蘭素史克(GSK)、默沙東、輝瑞(Pfizer)、賽諾菲被稱爲全球四大疫苗巨頭。每經小編(微信號:nbdnews)梳理這幾家公司財報發現,其研發費用占收入的比例分別爲
默沙東:18.20%;
葛蘭素史克:14.80%;
輝瑞:14.47%;
賽諾菲:15.6%;
與1.2億的研發投入相比,截至2017年,長生生物賬面上卻有20億元的理財産品。賬面上未分配利潤高達18.45億元。
2017年營業收入15.53億元,研發投入僅1.22億元,那麽,長生生物把錢都花哪了呢?其中的大頭是銷售費用——5.82億元,是研發投入的近5倍。
銷售費用是什麽呢?它包括推廣服務費、會議費、市場服務費、宣傳費、銷售職工的薪酬等等。
銷售人人員25人,平均每人的銷售費用2328萬元。
研發人員153人,平均每人的研發費用79.73萬元。
近日,針對長生生物疫苗問題,多家媒體提出質疑:
人民日報官方微博:連狂犬病疫苗也敢造假,既膽大包天,又傷天害理。幸虧所涉批次産品尚未上市銷售,否則後果不堪設想。疫苗關涉生命安全,來不得絲毫貓膩,容不得半點瑕疵,也使不得一點僥幸。用徹查還原真相,依法處理打消公衆恐慌,確保藥品安全。
《人民日報》:一查到底,方可纾解疫苗焦慮。疫苗事關生命健康,質量安全容不得半點瑕疵,不能有一點僥幸。此次疫苗事件引來廣泛關注之後,很多人在朋友圈曬出自家孩子的疫苗接種記錄,可見公衆對此事高度重視,也再一次提醒相關機構加強監管、提醒相關企業不要觸碰“紅線”。
《經濟參考報》:對疫苗造假決不能“罰酒三杯”了事。在一些網民看來,“這種企業不退市真的難消心頭之恨”。網民“趨勢巡航”稱,狂犬疫苗關乎生命,長生生物狂犬病疫苗生産記錄造假,被國家藥品監督管理局收回GMP證書,像這種無良無德的上市公司就應該直接退市,還要處罰到傾家蕩産。
中國之聲《新聞縱橫》四問長生生物百白破疫苗舊案:25萬支問題疫苗,加起來才罰了344.29萬元,質疑聲不少。多位法律界人士表示,我國目前對于類似違法違規行爲處置較輕,警示不夠。
《檢察日報》:長春長生發布聲明,表示已按要求停止狂犬疫苗的生産,並“深表歉意”。對此,很多人表示,這麽大的事不能僅僅“致歉”了事,應該“治罪”。
《南方都市報》:一家劣迹斑斑的疫苗企業,壟斷或參與瓜分國內相關領域的疫苗市場,不斷接到違規罰單的同時也不斷獲得生産資質、接到疫苗訂單,在曝出醜聞與領受“無痛”懲罰的拉鋸中,嬰幼兒的健康、公衆的生命安全長期身處險境。一度被“偶合反應”成功解套的疫苗質量問題,終究要直面生産與監管的全盤拷問,對涉事企業嚴懲之余也要追究其生産資質的獲取流程乃至監管的失守甚至懲處的寬縱。
四問長生生物百白破疫苗舊案:
25萬支劣藥去哪裏了?!
◎作者 | 央廣記者 莊勝春、楊鈞天、徐菁
◎來源 | 央廣網
據中國之聲《新聞縱橫》報道,長生生物狂犬病疫苗生産記錄造假風波尚未平息,7月19日一波又起,或者說是沉渣泛起——長生生物公告說,他們收到了吉林省食藥監局的行政處罰決定書,原因是長生生物全資子公司長春長生生産的一批“百白破”疫苗“效價測定”項不符合規定、是劣藥,罰沒款總計344.29萬元。
略顯蹊跷的是,吉林省食藥監局早在去年10月27日就已對此立案調查,這一事件當時也曾引發輿論關注。此外,作爲一家上市公司,長生生物卻從沒有在之前的公告及2017年年報中對此予以披露。
接種百白破疫苗是預防兒童白喉、破傷風和百日咳的有效措施。按照國家免疫程序,百白破疫苗需接種4劑次,分別于3、4、5月齡和18月齡各接種1劑次。
事關孩子的健康,有關此事的文章昨天開始廣泛轉發,不少母親的第一反應是“看看自己兒子的疫苗接種本”,憂慮聲和質疑聲不絕于耳。長生生物背後究竟有多少疑問待解?
01
一問:爲何時隔近9個月才公布處罰決定?
7月15日,國家藥監局通報了長生生物子公司長春長生狂犬病疫苗生産記錄造假問題,問題疫苗的蓋子因內部人舉報而揭開。吉林省食藥監局已收回其《藥品GMP證書》,同時叫停其狂犬疫苗的生産,有關調查仍在進行。截止上一個交易日,長生生物股票已連續5天跌停。
其間,另一個蓋子又被打開。7月19日,長生生物發布公告,收到關于“百白破”疫苗舊案的處罰決定書。
7月20日,吉林省食藥監局在官網公開了這一決定書,落款處日期是7月18號。
這一決定的作出,距離舊案立案,已過近9個月之久;而距離狂犬病疫苗事發,僅過了三天。
這樣的時間安排是出于怎樣的考慮?中國之聲記者昨晚多次撥打吉林食藥監局多位負責人電話,均無人接聽、或挂斷了記者來電。
02
二問:問題疫苗去哪兒了?
處罰決定書中寫道,沒收庫存的剩余疫苗186支。但在庫存之外,已有252600支問題疫苗銷售到山東省疾病預防控制中心。這些疫苗去哪了?
公開報道中,《新京報》一篇發表于去年11月5日的報道有所提及——報道引述山東食藥監局市場處負責人的話說:1、有關部門正開展召回工作;2、問題藥品已全部封存。3、這批藥安全性沒問題,是效價不達標,目前沒發現接種這批疫苗出現問題的案例。
關于安全性的說法,中國疾病預防控制中心有關專家給予證實:可能影響免疫保護效果,但接種安全性風險沒有增加。
但究竟有多少疫苗流入市場?是全部封存了,還是的確有孩子注射了問題疫苗、有多少?有沒有孩子因爲問題疫苗患病、健康受損?家長們如何判斷自己的孩子接種的是不是問題疫苗,有無救濟渠道?
中國之聲記者昨晚試圖就此詢問山東食藥監局有關負責人,沒有得到答複。國家市場監管總局方面則表示,周一再考慮就相關問題作出回應。
03
三問:長生生物是否有所隱瞞?
根據《上市公司信息披露管理辦法》:當公司涉嫌違法違規被有權機關調查,投資者尚未得知時,上市公司應當立即披露,說明事件的起因、目前的狀態和可能産生的影響。但直到三天前,長生生物才打破沉默,披露了處罰事項,並承認百白破生産車間已經停産。
另有《上海證券報》報道顯示,在長生生物2015年年報中,公司百白破批簽發量約562萬人份,位列公司在售6種疫苗産品之首。在2016年、2017年公司年報中仍稱,長春長生在售産品包括百白破疫苗等,但疫苗的批簽發量卻沒有披露。另一個變化是,百白破也消失在近兩年公司的在售産品圖片列表中。
究竟公司何時停止了百白破疫苗的生産?公告沒說。
昨天晚間,長生生物方面對外電話也均無人接聽。
7月20日,深交所發布關注函,要求長生生物對百白破生産車間已經停産涉及産品占公司營收的比重、對公司的具體影響以及公司擬采取的應對措施做出補充說明;另外,要求公司說明是否存在信息披露不及時的情形以及公司生産經營情況等其他事項。
在同一天的證監會例行新聞發布會上,證監會新聞發言人高莉也談及上市公司信息披露問題。她表示,隨著監管執法的不斷強化,近幾年上市公司財務信息的披露質量大幅提升,但其他類型重大事項的披露質量依然有待提升,凡屬可能對上市公司股票交易價格産生較大影響的重大事件,信息披露義務人均應依法及時披露,充分說明事件的起因、目前的狀態和可能産生的影響。下一步證監會將抓緊做好相關工作,對各種類型的信息披露違法行爲予以嚴厲打擊。
04
四問:吉林省食藥監局處罰是否過輕?
處罰決定書顯示,對于涉事百白破疫苗,共沒收違法所得85.88萬元,並處違法生産藥品貨值金額三倍罰款258.4萬元。
25萬支問題疫苗,加起來才罰了344.29萬元,質疑聲不少。
但處罰決定書中也明確了處罰依據——根據《藥品管理法》,生産、銷售劣藥的,沒收違法生産、銷售的藥品和違法所得,並處違法生産、銷售藥品貨值金額一倍以上三倍以下的罰款;劣藥以孕産婦、嬰幼兒及兒童爲主要使用對象的,在處罰幅度內從重處罰。
但另一方面,《藥品管理法》還規定,生産、銷售劣藥,情節嚴重的,責令停産、停業整頓或者撤銷藥品批准證明文件、吊銷相關許可證;構成犯罪的,依法追究刑事責任。
多位法律界人士告訴中國之聲,在現有法律框架內,三倍處罰的確已是“從重處罰”;至于是否“情節嚴重”,認定存在難度,暫無證據佐證涉事百白破疫苗造成了較大影響。不過,他們也同時表示,我國目前對于類似違法違規行爲處置較輕,警示不夠。
有資深律師建議,類似行爲應十倍處罰封頂,但他也坦誠,現行《藥品管理法》15年才修訂過,短時間內再修訂可能性不大。
這個公衆號內容還不錯,不如長按關注一下吧!
▼
這7篇文章你看了嗎?
▶今天新加坡被這道番茄炒蛋刷屏,結果有的人看哭了,有的人卻氣炸了……
▶新加坡護照又升級,終于晉升全球第一名!(免簽國最全列表供收藏)
▶來新加坡久了,你都變這副德行了!