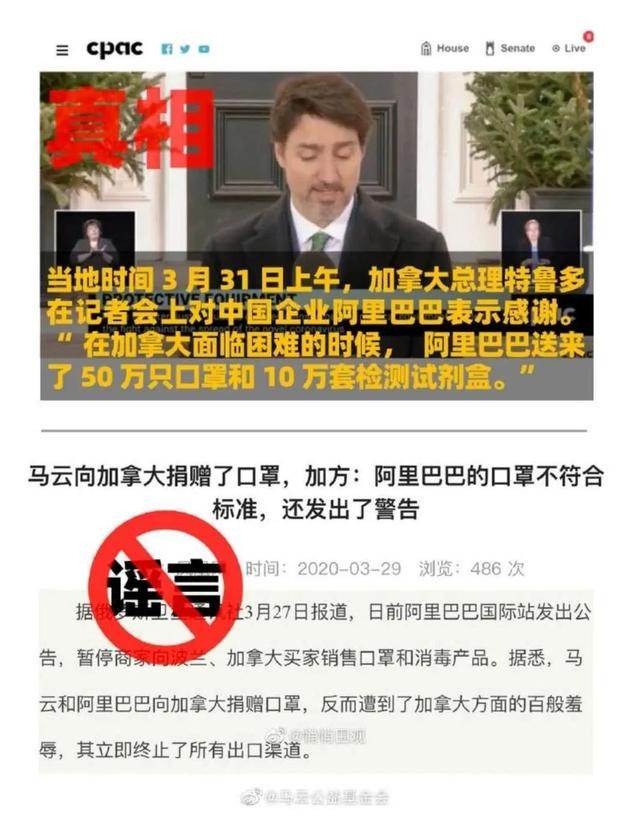
深圳易瑞生物在聲明中附上的CE證書
“易瑞生物是一家主營食品安全檢測的公司,並計劃在創業板上市,目前已經成爲行業的一條導火索。很多地方藥監局在查檢測公司,看是否有相關生産證書。”一位診斷試劑生産企業負責人向21新健康表示。
據21新健康了解,我國醫療器械産品出口,是依照《醫療器械産品出口銷售證明管理規定(原國家食品藥品監管總局2015年18號通告)》,其中一直有規定出口企業取得銷售國相關認證的同時,也要在我國取得醫療器械産品注冊證書及生産許可證書。
“醫療器械産品出口證書由國家藥監部門出具,若沒有在中國注冊生産的,藥監部門不出具,但企業如果有銷售國家認證,海關是認的,可以放出關。”上述企業負責人介紹說。
另一位接近藥監部門的業內人士向21新健康表示,此前僅有目的地國家的相關認證即可以出口,是疫情特殊情況下,海關、藥監提出的一個出口特殊通道。這個通道可能因爲一些企業的問題而關閉。
“據傳,早在3月16日國家藥監局就發布了依申請公開的文件,裏面提到疫情物資出口企業需要獲得中國主冊生産資質,但各省藥監部門一直沒有公開,可能也是有對出口企業的考量。” 上述接近藥監部門的業內人士表示。
不過,負面影響還是來了。
上述負責人表示,受3月31日晚最新規定影響,很多只有歐盟、美國等國家認證,沒有獲得國內生産注冊的企業,不能再出口,多家生産企業、外貿商遭受巨大打擊。“我們希望企業出口做好自律,不要因爲貪圖眼前利益,對整個行業造成毀滅性的打擊。”
史立臣也指出,除了標准問題,産品質量仍是關鍵,不管是企業出口銷售還是捐贈,如果質量出現問題,不僅會影響中國制造的口碑,也可能會引發企業訴訟等。
21新健康向全體讀者征稿!
不管您是醫護人員,還是患者、患者家屬,或是相關企業從業人員,只要您了解與本次疫情相關的信息與情況,或有想講述的故事,都請與我們聯系!
21新健康編輯微信:sanadamo(請附言“投稿”)
投稿郵箱:[email protected]