骨質疏松症(Osteoporosis,OP)是一種骨骼代謝性疾病,主要表現爲骨量減少、骨微觀結構退行性變化,常伴隨有長期疼痛、骨質疏松性骨折等並發症。OP按病因可分爲原發性和繼發性兩類,其中原發性OP又分爲I型和II型,前者即絕經後骨質疏松症,見于絕經後女性,後者即老年骨質疏松症,見于老年人;繼發性OP常由內分泌代謝疾病或全身性疾病引起。本文聚焦原發性I型(絕經後骨質疏松症)與II型(老年骨質疏松症)。
骨質疏松症危害高于普遍認知
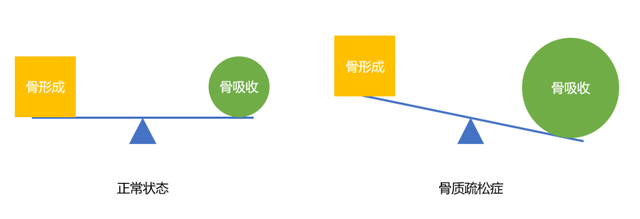
1.1 發病機制簡介:骨形成與骨吸收失衡
長期以來,公衆對于骨質疏松症發病的認識都停留在缺鈣、缺維生素D的問題上,但事實上,盡管鈣和維生素D確實是防治OP的基礎用劑,其發病機制卻遠比此複雜。了解骨質疏松症的發病機制不得不提到兩個概念——骨形成和骨吸收。骨形成是新骨形成的過程,與人體中的成骨細胞密切相關;而骨吸收是骨質被分解吸收的過程,與破骨細胞密切相關。
正常狀態下,骨形成和骨吸收的過程在骨骼中形成動態平衡,保證骨骼的構建、塑形和重建,使骨骼具有足夠的剛性和韌性維持骨強度。但隨著年齡的增長,骨形成和骨吸收之間的平衡被打破,破骨細胞較成骨細胞更爲活躍,使得骨吸收強于骨形成,從而骨總量減少、骨強度降低,導致骨質疏松症。
1.2 流行病學概覽:骨質疏松症已成爲重要公共健康問題
骨質疏松症的患病率與增齡高度相關,且危害巨大,患者骨脆性增加、骨強度降低,發生骨折的風險大幅上升。OP及骨折的醫療和護理需要投入大量的人力、物力和財力,帶來沉重的家庭負擔和社會負擔。隨著人口老齡化日趨嚴重,骨質疏松症更是逐漸成爲我國面臨的重要公共健康問題。
1.2.1 中老年人群發病率
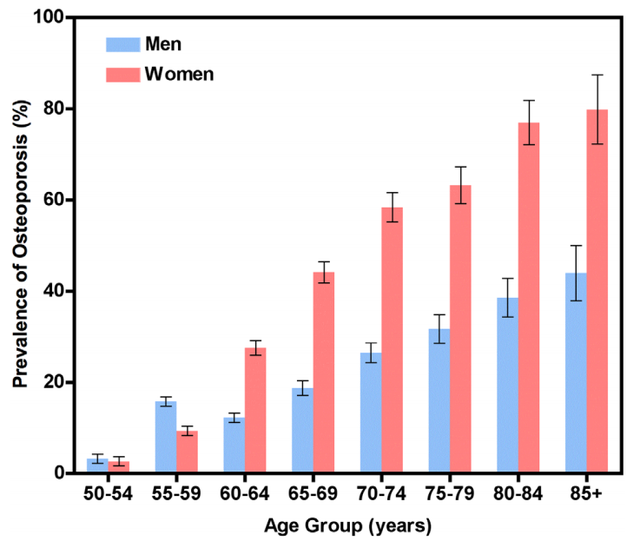
根據2020年全國多家醫療中心數據,目前我國50歲以上老年男性和女性的骨質疏松症發病率分別爲13.5%和29%,這意味著,每八名50歲以上男性中即有一名骨質疏松症患者,每四名50歲以上女性中即有一名骨質疏松症患者。
隨著年齡增長,男性和女性的骨質疏松發病率均顯著增加,從60歲起,女性發病率幾乎爲同年齡男性的2倍,可見中老年女性骨質疏松問題尤爲嚴重。
1.2.2 並發症發病率與生存率
骨質疏松性骨折是骨質疏松症最嚴重的並發症,該類骨折好發于椎體、髋部等松質骨含量較高的部位,可導致畸形、殘疾,甚至死亡。研究指出,女性一生發生骨質疏松性骨折的危險性(40%)高于乳腺癌、子宮內膜癌和卵巢癌的綜合,男性一生發生骨質疏松性骨折的危險性(13%)高于前列腺癌。
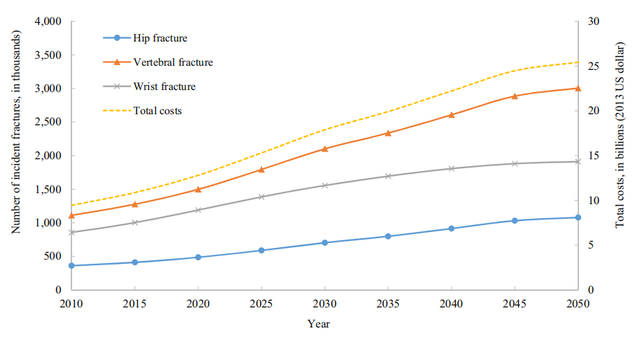
近年來,骨質疏松性骨折的發生率在逐年增加,據預測,2030年我國主要骨質疏松性骨折(腕部、椎體和髋部)約爲436萬例次,所花費醫療費用將高達1185億元,到2050年約達599萬例次,醫療費用達1630億元。
在各類骨質疏松性骨折中,髋部骨折有較高的致殘率和致死率。發生髋部骨折後一年之內,五分之一的患者會死于各種並發症,二分之一的患者會留下殘疾,生活質量下降,未來生存率明顯惡化。
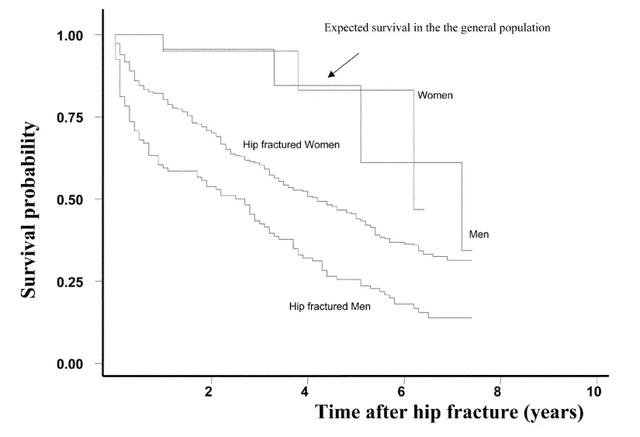
盡管女性有著更高的骨質疏松症發病率,男性發生髋骨骨折的概率卻高于女性。並且,瑞士研究表明,在發生髋骨骨折的一年後,男性生存率大幅低于女性生存率,兩者生存率在一年後則逐漸趨于平行,至研究跟蹤期(7年)結束,男性生存率僅15%,而女性則爲33%。
1.2.3 住院醫療費用統計
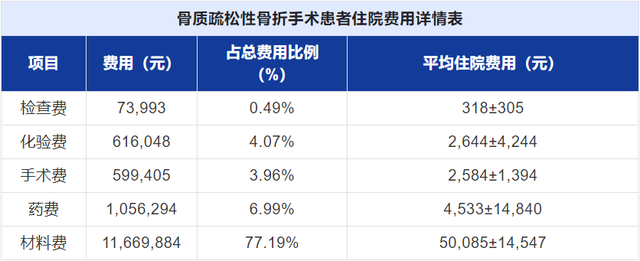
骨質疏松性骨折在造成患者極大的身心負擔的同時,也爲家庭帶來了沉重的經濟負擔。2019年,一項北京協和醫院的骨質疏松性骨折手術患者住院費用統計分析表明,患者的平均住院費用高達60,164元,其中材料費(包括術中耗材及假體費用)占比超過70%,藥費及化驗費位居第2、3位,總共占比約10%。
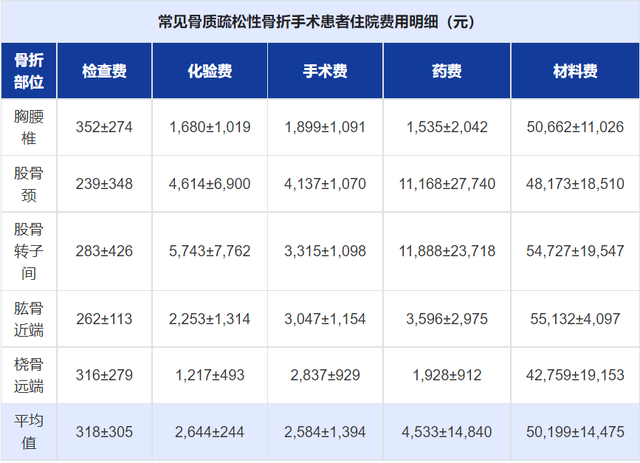
根據骨折部位的不同,其住院費用明細統計如下。
可以看到,股骨頸骨折和股骨轉子間骨折(兩者爲髋部骨折的主要類型)的平均住院費用約爲68,331元和75,956元,高于其他常見骨質疏松性骨折平均住院費用(4,000元到17,000元不等)。
該分析同時指出,當患者患有慢性基礎疾病(高血壓、冠心病、糖尿病等)時,其平均住院費用明顯增加,特別是化驗費與藥費。有基礎疾病患者的平均住院費用爲67,673元,無基礎疾病患者的平均住院費用則爲56,865元,低于前者10,808元。
骨骼健康有賴于長期防治管理
骨質疏松症的發生與基礎骨量積累和後期骨量流失密切相關,社會大衆對骨質疏松症認知水平不高、早期預防措施缺失及篩查率低亦是導致我國患者人群龐大的重要原因。根據國家衛健委2018年發布的流行病學調查結果,我國50歲以上人群的骨密度檢測比例僅爲3.7%,患病知曉率僅爲7%。
2.1 早期預防:延緩骨量丟失
通常來說,人體在30歲前後達到一生中的骨量峰值,進入中年之後骨量開始緩慢丟失。女性從40歲~49歲起進入骨量丟失前期,年丟失率爲0.4%~0.6%,絕經後1年至10年則進入骨量快速丟失期,年丟失率上升至1.5%~2.5%;男性的骨量丟失速度相對緩慢,通常從40歲~64歲進入骨量丟失前期,年丟失率保持在0.3%~0.5%。女性一生將丟失骨總量的50%左右,男性一生將丟失骨總量的30%左右。
低骨量往往沒有明顯的臨床表現,加之我國居民骨密度檢測率較低,導致大部分居民在骨量下降初期沒有及時采取防控措施,而在出現疼痛、脊柱變形和骨折等情況後才發現患病,延誤了骨松防治的有利時機。因此,盡早識別風險、延緩骨量丟失尤爲重要。
2.1.1 低骨量風險可于早期自查
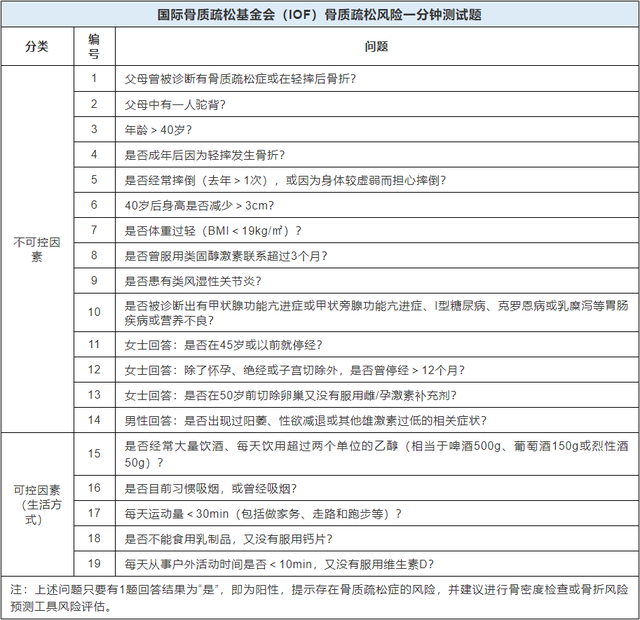
我國《低骨量診療專家共識(2014)》選用了兩種初篩工具對低骨量臨床危險因素進行評估,其中國際骨質疏松基金會(IOF)的一分鍾測試題較爲常用,方法是根據病史初步篩選出可能具有骨質疏松風險的患者。
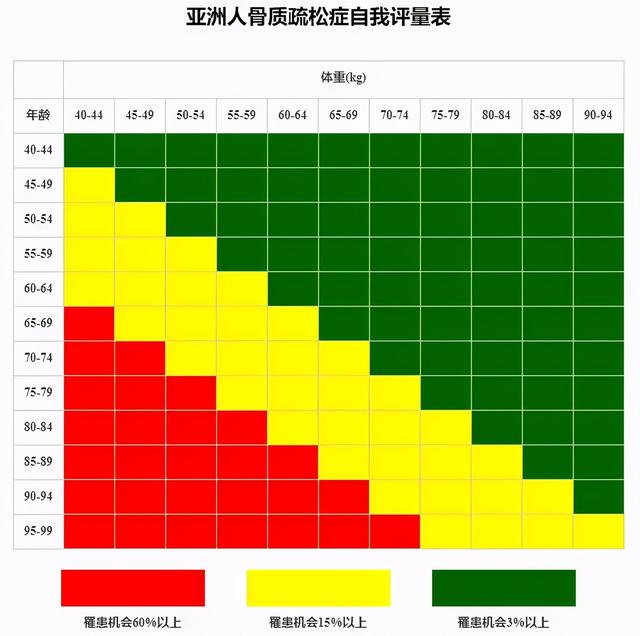
另一種是亞洲人骨質疏松自我篩查工具(OSTA),主要根據年齡和體質量篩查骨質疏松症的風險,計算方法爲[體重(kg)-年齡(歲)]×0.2。其特異性不高,僅適用于絕經後婦女。
2.1.2 基礎預防措施應貫穿始終
骨質疏松症的基礎預防措施包括調整生活方式與攝入骨健康補充劑。進入骨量流失期後,一方面需攝入富含鈣、低鹽和適量蛋白質的均衡膳食,《中國居民膳食指南》推薦每日攝入蛋白質0.8~1.0g/kg、牛奶300ml或相當量的奶制品;同時,保證每周接收2次充足日照(上午11:00到下午3:00間,盡可能多地暴露皮膚于陽光下曬15~30min),以促進體內維生素D的合成;堅持負重與抗阻運動,練習肌肉力量,以增加骨密度、減少骨折風險;此外也應戒煙、限酒、避免過量飲用咖啡及碳酸飲料,避用或少用影響骨代謝的藥物。
另一方面,骨質疏松症風險人群還需補充攝入鈣劑和維生素D。營養調查顯示,我國居民每日膳食中攝入元素鈣約400mg,而建議總攝入量爲每日800mg,50歲及以上人群更應達到1000~1200mg;健康成年人維生素D的推薦攝入量爲400U(10μg)/ 日,用于骨質疏松症防治時,劑量可增加至800~1200 U / 日。
2.1.3 健康服務平台探索解決方案
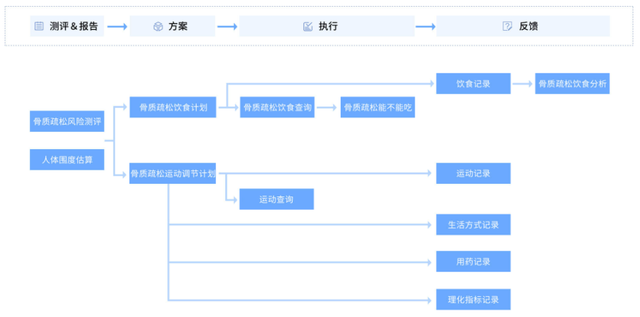
第三方健康服務平台也已開始嘗試骨質疏松症的預防管理,下圖是一個典型的骨松風險人群管理方案:從飲食、運動、生活方式、身體數據等維度對用戶進行測評,輸出骨質疏松高中低風險等級,並基于評級制定個性化飲食計劃、運動調節計劃;在方案執行過程中,通過日常的飲食、運動、生活方式、用藥、理化指標記錄對方案進行有效反饋;同時,提供相關的查詢、分析及其他信息獲取工具。
2.2 中期防治:抑制骨吸收、降低骨轉換率,防止意外骨折
2.2.1 定期骨密度篩查必不可少
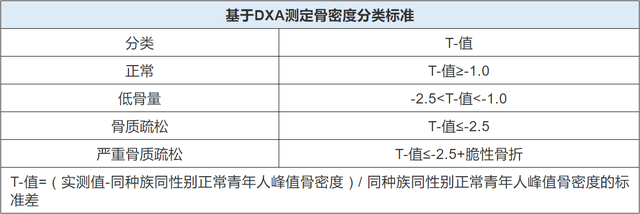
隨著年齡增長,50歲以上人群的骨質疏松風險顯著增加,尤以65歲以上女性患病幾率最高。定期進行骨密度篩查是中老年人群識別骨質疏松風險、盡早開展診療的必要手段,《中國防治慢性病中長期規劃(2017-2025年)》中已將骨密度檢查項目納入40歲以上人群的常規檢查。目前,DXA測量的骨密度是最爲通用的骨質疏松症診斷指標。
2.2.2 抗骨質疏松常用藥已入醫保
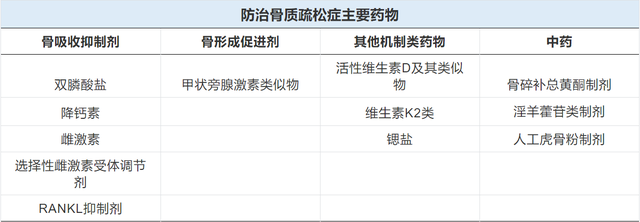
除基礎預防措施之外,抑制骨吸收、降低骨轉換率是老年群體防治骨質疏松症的重點,必要時可使用抗骨質疏松藥物。抗骨質疏松症藥物按作用機制可分爲骨吸收抑制劑、骨形成促進劑、其他機制類藥物及傳統中藥。通常首選使用具有較廣抗骨折譜的藥物(如阿侖膦酸鈉、利塞膦酸鈉)。對低、中度骨折風險者,如年輕的絕經後婦女、骨密度水平較低但無骨折史的人群,首選口服藥物治療。對口服不能耐受、禁忌、依從性欠佳及高骨折風險者,如骨密度水平極低的患者,可使用注射制劑(如唑來膦酸)。
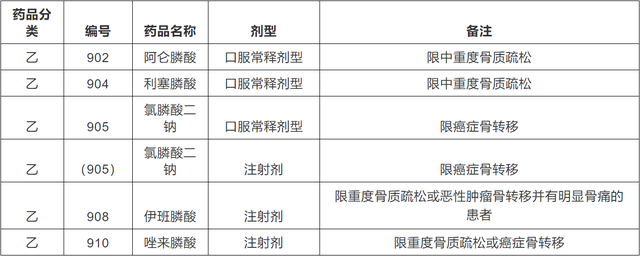
雙膦酸鹽是目前臨床上應用最爲廣泛的抗骨質疏松症藥物,主要包括阿侖膦酸鈉、唑來膦酸、利塞膦酸鈉、伊班膦酸鈉和氯膦酸二鈉等,均已納入國家基本醫保藥品目錄(乙類)。
△資料來源:《國家基本醫療保險、工傷保險和生育保險藥品目錄(2020年)》
然而,大部分傳統藥物在多年使用之後在預防骨折方面會達到治療平台期,並且都可能導致一定的不良反應,例如雷奈酸锶等藥物可能增加心肌梗死的風險,在老年人群的骨質疏松症治療中已較少使用;臨床上急需效果更佳、使用方便的新型藥物。
2020年,國家藥監局批准新型RANKL抑制劑地舒單抗用于絕經後骨折高風險女性的骨質疏松症治療,該藥物可抑制破骨細胞的形成和骨吸收功能。其治療相對安全,具有較低的不良反應發生率,可用于腎功能異常的患者;且使用方便,患者對其治療有較高的滿意度和依從性,半年一次皮下注射爲需要長期使用其他藥物的慢性病患者提供了便利。
2.2.3 保險業關注老年骨折風險
中保協《中國保險人群意外傷害風險研究報告(2017)》表明,老年人的總體意外傷害風險高于中青年,跌倒、墜落是50周歲以上人群首要的意外傷害風險因素。
針對老年群體骨質疏松症患病率高、易因意外摔倒而引發骨折及傷殘的現狀,近年來,保險行業已開始探索老年骨折意外險+健康管理模式,其典型形態是:在意外身故/傷殘、意外醫療與住院津貼等常規保險責任上增加意外骨折定額給付責任,若被保險人因意外事故導致骨折,保司將根據骨折嚴重程度給付不同比例的醫療補償金,首次投保年齡可至75歲或更高。同時,保單贈送老年人專屬體檢、120急救協助、骨折康複咨詢等相關健康服務,覆蓋老年人意外骨折的預防、治療與康複全階段。
2.3 骨折後療養:治療與康複、防止二次骨折
2.3.1 治療與康複減輕骨折疼痛
如已發生骨質疏松性骨折,條件允許的情況下,應盡早對患者進行手術治療以減輕疼痛,同時輔以康複鍛煉以降低手術後並發症發生的風險,提高患者生存率。針對不同部位的骨折,有不同的手術治療方式:
但考慮到骨質疏松性骨折患者多爲老年人,常合並其他疾病,不能耐受麻醉和手術的情況較多,可采用括臥床、牽引、支具固定、營養支持等治療措施。
在治療骨折的同時,也需重視抗骨質疏松治療。一般來說,待患者身體狀況和創傷反應穩定後,應適時進行抗骨質疏松藥物治療,包括骨吸收抑制劑或骨形成促進劑等。骨質疏松性骨折的恢複慢,康複期長;在不影響骨折制動及骨折愈合的前提下,應盡早開始康複訓練,恢複關節運動功能,減少肌肉萎縮,增強肌肉力量,促進骨折愈合和防止再發骨折。
2.3.2 骨折聯絡服務防範二次骨折
骨折聯絡服務(Fracture Liaison Services,FLS)是一種規範化管理已發生骨質疏松性骨折患者的系統幹預方法,已成爲全世界預防二次骨折發生的主要途徑。通過在門診和住院部建立骨折聯絡服務,可以系統地識別和治療骨折患者,並幫助預防二次骨折的發生,從而降低骨折後患者病死率和巨大醫療費用。
FLS由多學科協作團隊提供,包括衛生系統骨質疏松症臨床醫生(通常是內分泌、風濕病、老年病學醫生)、骨科醫生、老年病或老年創傷醫生、放射科醫生、相關專科護士、物理治療師和其他專職醫療保健專業人員、跌倒機構、負責開發FLS數據的IT人員等。FLS成功的核心是骨折聯絡協調員,負責識別及評估骨質疏松性骨折患者,並對其進行健康教育同時啓動治療。
在亞太地區,最具代表性的當屬新加坡中央醫院開展的二次骨折管理系統,該系統以骨質疏松症患者爲主要目標人群,旨在爲患者提供綜合管理建議以提高其健康質量。調查顯示在新加坡超過50%的醫院都已開展骨折聯絡服務,這一成果在全世界範圍內也屬領先水平。目前,中國大陸已在醫院系統內,針對50歲以上人群開展了類似的骨折聯絡服務。
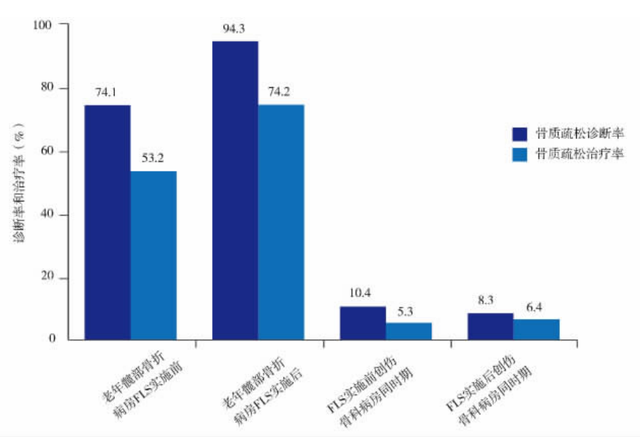
2017年北京積水潭醫院的一項調研顯示,在實施FLS後,老年髋部骨折病房的患者的骨質疏松症診斷率與治療率均高于FLS實施前,這意味著FLS治療模式在老年髋部骨折患者的骨質疏松症診斷與治療方面展示出了明顯的優勢。長期來看,鑒于目前我國的快速老齡化現狀和骨質疏松性骨折的嚴峻形勢,期待FLS在國內能夠在預防二次骨折上發揮更大的作用。
參考文獻:
[1] 中華醫學會骨質疏松和骨礦鹽疾病分會. 原發性骨質疏松症診療指南 (2017) [J]. 中國骨質疏松雜志, 2019, 25(3), 281-309.
[2] 中華醫學會全科醫學分會. 原發性骨質疏松症基層診療指南 (2019年) [J]. 中華全科醫師雜志, 2020, 19(4), 304-315.
[3] 李曾, 常曉, 王英傑,等. 骨質疏松性骨折手術患者住院費用統計分析[J]. 中華骨與關節外科雜志, 2019(10).
[4] 王亮. 低骨量診療專家共識 [C]. 中國骨質疏松雜志社. 2014.
[5] 中國營養學會. 中國居民膳食指南2016 [M]. 北京: 人民衛生出版社, 2016.
[6] 中國營養學會. 中國居民膳食營養素參考攝入量速查手冊 [M]. 北京: 中國標准出版社, 2014.
[7] 羅鳳基. 健康生活小百科——防病知識 [M]. 北京: 人民衛生出版社出社, 2011.
[8] 邱貴興, 裴福興, 胡偵明,等. 中國骨質疏松性骨折診療指南(全文)(骨質疏松性骨折診斷及治療原則)[J]. 中華關節外科雜志:電子版, 2015, v.9(06):117-120.
[9] 李甯, 楊明輝, 李新萍,等. 老年髋部骨折中”骨折聯絡服務”的初步臨床效果[J]. 骨科臨床與研究雜志, 2017, 002(005):P.287-292.
[10] Cheng, X., Zhao, K., Zha, X., et al. Opportunistic Screening Using Low‐Dose CT and the Prevalence of Osteoporosis in China: A Nationwide, Multicenter Study[J]. Journal of Bone and Mineral Research.
[11] Trombetti, A., Herrmann, F., Hoffmeyer, P., et al. Survival and potential years of life lost after hip fracture in men and age-matched women[J]. Osteoporosis International, 2002, 13(9), 731-737.
[12] Si L , Winzenberg T M , Jiang Q, et al. Projection of osteoporosis-related fractures and costs in China: 2010–2050[J]. Osteoporosis International, 2015.
[13] BONE H G, WAGMAN R B, BRANDI M L, et al. 10 years of denosumab treatment in postmenopausal women with osteoporosis: results from the phase 3 randomised FREEDOM trial and open-label extension [J]. The lancet Diabetes & endocrinology, 2017, 5(7), 513-523.
[14] FREEMANTLE N, SATRAM-HOANG S, TANG E T, et al. Final results of the DAPS (Denosumab Adherence Preference Satisfaction) study: a 24-month, randomized, crossover comparison with alendronate in postmenopausal women [J]. Osteoporosis international, 2012, 23(1), 317-326.